Comment les chercheurs conçoivent-ils un médicament contre le cancer qui restaure la réponse immunitaire ?
Le système immunitaire joue un rôle clé dans la lutte contre le cancer: il traque et élimine les cellules cancéreuses. Mais ces dernières déploient toute une série d’astuces pour échapper à sa vigilance.De nombreuses cellules cancéreuses produisent la protéine indoleamine 2,3-dioxygenase 1 (IDO1) en grande quantité. Un taux élevé d’IDO1 dans une tumeur est souvent lié à un mauvais pronostique. Pourquoi? IDO1 est une protéine impliquée dans la dégradation de l'acide aminé tryptophane. Le tryptophane est un acide aminé essentiel: il doit être en quantité suffisante pour que les cellules puissent se diviser normalement. Dans l’environnement d’une cellule cancéreuse produisant IDO1 en grande quantité, la baisse de la concentration de tryptophane entraîne un arrêt de la prolifération des cellules du système immunitaire (lymphocytes T). De plus, certains produits dérivés de la dégradation du tryptophane sont directement toxiques pour les lymphocytes T.
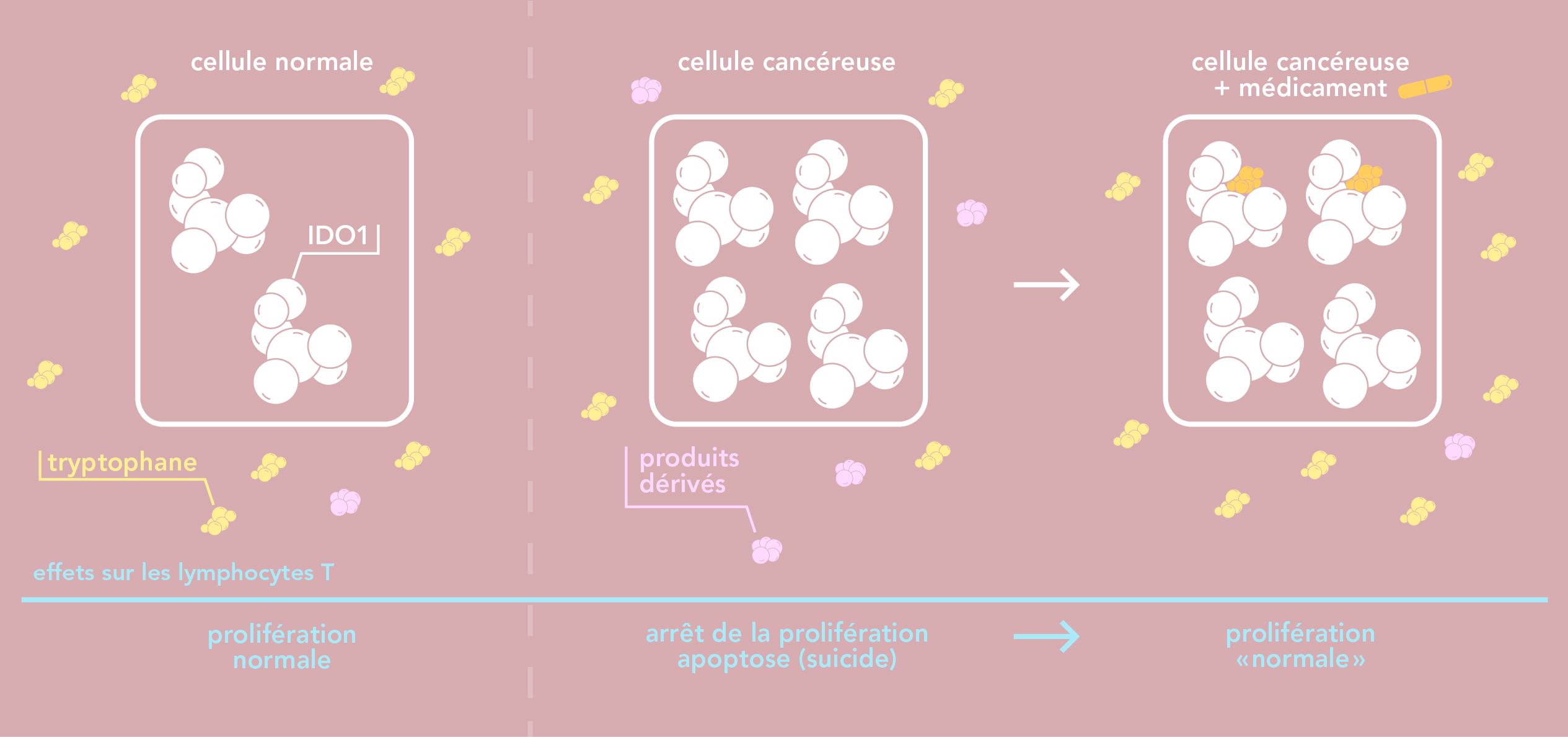
IDO1, exprimée en grande quantité, permet donc aux tumeurs d’échapper aux défenses immunitaires naturelles. IDO1 permet également aux tumeurs de résister aux défenses immunitaires induites dans le cadre d’une immunothérapie - un nouveau traitement anti-cancéreux qui s'ajoute aux traitements traditionnels tels que la chimiothérapie ou la radiothérapie. C’est la raison pour laquelle IDO1 est une cible thérapeutique prometteuse pour le traitement du cancer: l’inhibition d’IDO1 augmente l’efficacité des immunothérapies et ainsi que d'autres traitements en restaurant la réponse immunitaire. Le développement de molécules qui inhibent spécifiquement cette protéine est ainsi devenu l’objet d’une recherche intensive depuis le début des années 2000.
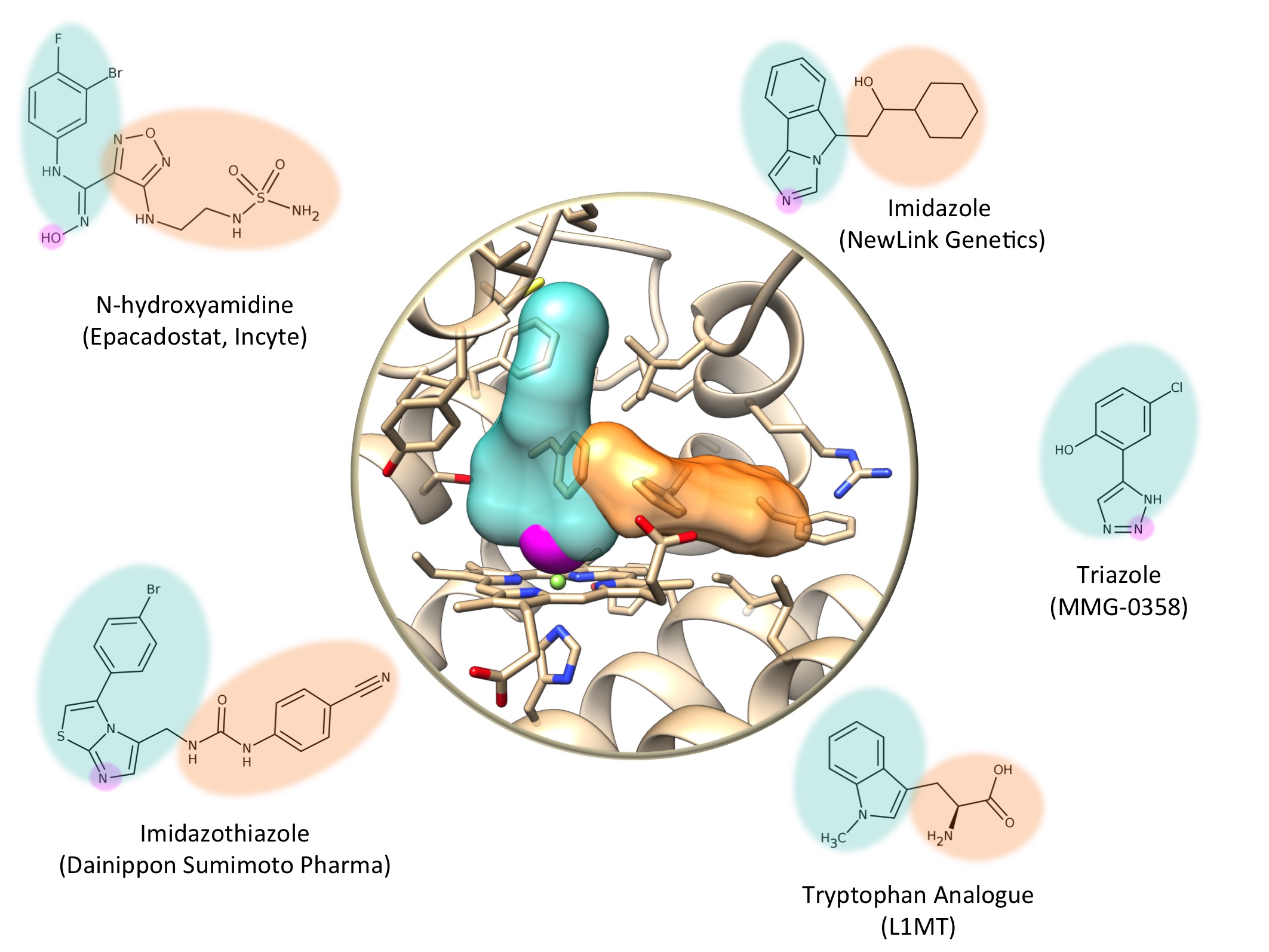
Les premiers inhibiteurs d'IDO1 étaient des analogues du tryptophane, le substrat naturel de la protéine. D’autres chercheurs ont découvert des inhibiteurs par criblage de librairies de molécules sur des cultures cellulaires. La découverte de la structure 3D d'IDO1 par cristallographie, en 2006, a permis le conception de nouvelles molécules, conçues à l’aide de modèles informatiques (‘computer-aided structure-based drug design’). Par exemple, au SIB Institut Suisse de Bioinformatique, des chercheurs ont développé plusieurs dizaines de molécules dérivées du triazole, dont une, appelée MMG-0358, semble très prometteuse.
Voici quelques exemples de molécules ayant le potentiel de devenir un médicament anti-cancéreux:
Remarque : IDO1 est impliqué dans de nombreux processus physiologiques ou pathologiques impliquant une réponse immunitaire: infections chroniques, inflammation, transplantation, tolérance maternelle envers le fœtus, maladies autoimmunes et allergies. Les inhibiteurs d'IDO1 pourraient donc être aussi développés pour le traitement de différentes maladies, en plus du cancer, comme les maladies neurodégénératives (Alzheimer, Parkinson, Huntington, sclérose amyotrophique, ...) ou certaines infections (HIV, tuberculose, ...)
Cet atelier permet de découvrir comment la bioinformatique:
- aide à concevoir une molécule qui cible spécifiquement IDO1, en utilisant la technique du molecular docking. Cette technique permet de prédire comment la molécule se lie à une protéine (structure 3D) ainsi que la force de cette liaison (calcul d’un score),
- permet de prédire la ou les protéines cible(s) du médicament (SwissTargetPrediciton),
- permet de prédire le devenir d’une petite molécule dans le corps humain (SwissADME: Absorption, Distribution, Métabolisme et Excrétion).
Vous pourrez comparer les prédictions d’efficacité, de sécurité et de spécificité de la molécule que vous avez dessinée avec les molécules suivantes:
- AMG-1, un imidazothiazole développé par Dainippon Sunimoto Pharma.
- MMG-0358, un triazole développé par le SIB Institut Suisse de Bioinformatique. MMG-0358 a une forte affinité pour IDO1 et est actif in vivo.
- PIM, un imidazole. PIM est l'un des premiers inhibiteurs d'IDO1 dont la structure 3D en complexe avec IDO1 a été obtenue. PIM a une faible affinité pour IDO1 et est peu spécifique.
- L1MT, ou L-1-methyltryptophane, un analogue inerte du tryptophane qui inhibe IDO1. L1MT est en cours d'évaluation clinique pour le traitement des cancers du sein et de la prostate.
- NLG-919, un imidazole développé par NewLink Genetics. NLG-919 est actuellement en cours d'évaluation clinique pour le traitement de tumeurs solides.